가톨릭대학교 여의도성모병원 소화기내과 양경모 교수, 카이스트 정원일 교수, 서울대학교 보라매병원 김원 교수 연구팀이 알코올성 간질환의 핵심 발병 메커니즘을 세계 최초로 규명했다. 이번 연구는 ‘폭음 시 간세포가 글루타메이트를 분비하여 면역세포와 직접 소통하며 염증을 유발한다.’는 발견으로, 알코올성 간질환의 새로운 치료 전략 수립에 중요한 단서를 제공할 것으로 기대된다.
 폭음이 촉발하는 간세포-면역세포 간 염증성 신호전달 최초 규명
폭음이 촉발하는 간세포-면역세포 간 염증성 신호전달 최초 규명
연구팀은 만성 음주에 노출된 간세포가 평소 VGLUT3(소포성 글루타메이트 수송체 3)를 통해 글루타메이트를 세포 내 소포에 저장하고 있다가, 폭음 상황에서
▲(좌부터) 여의도성모병원 소화기내과 양경모 교수,
카이스트 김규래 박사과정, 카이스트 정원일 교수, 서울대 보라매병원 김원 교수.
세포 내 칼슘 농도 변화로 인해 이를 급격히 방출한다는 사실을 밝혀냈다.
특히 주목할 점은 분비된 글루타메이트가 간의 대식세포인 쿠퍼세포의 mGluR5 수용체를 활성화하여 NADPH oxidase 2(NOX2)를 통한 활성산소종 생성과 염증 반응을 유발한다는 것이다. 더 나아가 알코올로 인해 부풀어 오른 간세포가 쿠퍼세포와 물리적 접촉을 강화하며, 이를 통해 신경세포 간 시냅스와 유사한 '의사시냅스(pseudosynapse)'가 형성됨을 확인했다.
양 교수는 "이는 간세포와 면역세포 간 직접적인 물리적·기능적 소통 경로를 보여주는 최초의 연구 결과"라며 "알코올성 간질환이 단순한 간세포 독성이 아니라 세포 간 복합적 상호작용에 의해 진행됨을 입증한 것"이라고 설명했다.
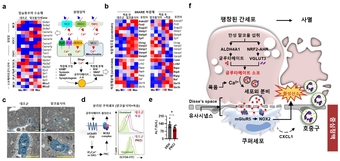
<표. 폭음에 의해 유도되는 글루타메이트 신호 경로를 통한 간세포-쿠퍼세포 간 상호작용과 알코올성 간질환 발병 기전>
임상 환자 검체 분석으로 메커니즘 검증, 치료 표적으로 주목
이번 연구는 동물모델과 세포 실험을 통해 제시된 결과를 실제 국내 알코올성 간염 환자의 혈액과 간 조직 검체를 활용하여 임상적으로 검증했다는 점에서 더욱 의미가 크다.
알코올성 간질환 환자에서는 혈중 글루타메이트 농도 상승, VGLUT3 발현 증가, 염증성 사이토카인 유도 등이 뚜렷하게 확인되었으며, 이는 해당 경로가 실제 임상 질환 발현과 밀접한 관련이 있음을 시사한다.
더욱 고무적인 것은 연구팀이 유전학적 및 약리학적 방법을 통해 VGLUT3 또는 mGluR5를 억제했을 때 간염과 간세포 손상이 유의미하게 완화됨을 확인했다는 점이다. 이는 이 경로가 알코올성 간질환의 유망한 치료 표적이 될 수 있음을 강력히 시사한다.
양경모 교수는 "이번 연구를 통해 간세포 내 글루타메이트 대사 조절이 단순한 대사 기능을 넘어 면역세포와의 직접적인 염증 소통 메커니즘에 관여함을 새롭게 규명했다"고 밝혔다.
이어 "향후 이 경로를 기반으로 한 조기 진단 바이오마커 개발이나 약물 표적 치료 전략이 활발히 이어지기를 기대한다"며 "특히 혈중 글루타메이트 농도 측정을 통한 조기 진단법 개발과 VGLUT3 또는 mGluR5를 표적으로 하는 새로운 치료제 개발이 가능할 것"이라고 전망했다.
이번 연구 결과는 네이처 커뮤니케이션즈(Nature Communications, IF 15.7) 2025년 7월호에 게재됐다.