광주과학기술원(GIST·지스트, 총장 임기철)은 화학과 김민곤 교수 연구팀이 다양한 질환의 표적 유전자를 유연하게 설계·검출할 수 있는 차세대 유전자 진단 기술을 제시했다고 30일 밝혔다.
 이 기술은 진단이 필요한 ‘타깃 유전자’를 대상으로 맞춤형 진단 방법을 설계할 수 있어 감염병·암·유전병 등 다양한 질환 진단에 적용될 수 있다.
이 기술은 진단이 필요한 ‘타깃 유전자’를 대상으로 맞춤형 진단 방법을 설계할 수 있어 감염병·암·유전병 등 다양한 질환 진단에 적용될 수 있다.
몸이나 바이러스에 포함된 유전 정보(DNA 또는 RNA)를 기반으로 질병을 진단하는 유전자 기반 진단 기술은 다양한 질환의 진단에 널리 쓰이고 있다.
▲(뒷줄 왼쪽부터) 화학과 이호연 연구교수, 이규한 석사과정생, 박준혁 박사과정생, 박여진 박사과정생
(앞줄 왼쪽부터) 박형빈 석박통합과정생(제1저자), 김민곤 교수(교신저자), 윤지영 석사과정생
현재 표준 진단 방법으로 사용하는 유전자 증폭 검사(Polymerase Chain Reaction, PCR)는 높은 정확도와 민감도를 나타내지만 시간이 오래 걸리고 전문적인 장비와 인력이 필요하다는 한계가 있다.
이러한 한계를 보완하기 위해 질병과 관련된 특정 유전자를 표적하는 ‘유전자 가위(CRISPR)*’와 일정한 온도에서 유전자를 빠르고 많이 복제하는 ‘등온 증폭 기술(Isothermal amplification)*’을 결합한 ‘단일 반응 진단법(One-pot CRISPR)*’이 주목받고 있다.
그러나 이 기술들은 유전자를 찾아내서 신호를 내는 반응 속도가 다르고 이를 조절하기 어려워, 유전자마다 최적 조건을 찾기 어렵고 설계의 유연성이 제한되는 한계가 있다.
* 유전자 가위(CRISPR): 특정 유전자 부위를 인식해 유전자 정보(DNA) 또는 유전 정보 전달 물질(RNA)을 선택적으로 자르는 효소 기반 기술이다. 세균의 면역 체계에서 유래해 침입한 유전 정보를 표적으로 제거하는 기능으로, 높은 표적 특이성을 바탕으로 원하는 유전자만 정확히 찾아내서 신호를 내는 것이 가능하다.
* 등온 증폭 기술(Isothermal amplification): 일반적인 유전자 검사처럼 온도를 계속 바꾸지 않고, 단일 온도에서 유전 정보를 담고 있는 분자(핵산)를 증폭하는 기술이다. 단일 반응 진단법(One-pot CRISPR)에서는 민감도를 높이는 역할을 하지만 비특이적인 증폭이 많이 일어난다.
* 단일 반응 진단법(One-pot CRISPR): 유전자 증폭과 유전자 가위(CRISPR) 표적 탐지를 하나의 시험관에서 동시에 진행하는 방식이다. 이 기술은 검사 과정을 단순화하고 오염 위험을 줄이지만, 증폭 및 탐지 과정의 최적화 극복이 핵심 과제이다.
연구팀은 이러한 한계를 해결하기 위해, 유전자 가위 기술을 제어하여 질환의 유무를 진단하는 ‘타깃 유전자’를 범용적으로 검출할 수 있는 새로운 접근법을 제시했다.
유전자 가위 기술에서는 마치 차량에서 내비게이션의 역할을 수행하는 가이드(RNA, 리보핵산)가 타깃 유전자를 찾으면 실제로 움직이는 엔진(유전자를 자르는 역할을 하는 Cas 단백질)이 그 유전자 부위에서 유전자를 자르며 신호를 발생시킨다.
연구팀은 여기에 속도를 조절하는 브레이크와 같은 역할을 하도록 길이가 짧은 ‘유전자 조각(올리고·oligo)’를 도입해 유전자를 자르고 신호를 내는 과정의 속도를 독립적으로 조절할 수 있도록 했다.
연구팀이 유전자 모델을 이용해 길이가 다른 올리고를 적용한 실험에서, 올리고 길이에 따라 브레이크의 강도가 달라지듯 반응 속도가 정밀하게 조절되는 것을 확인하고, 이를 바탕으로 최적의 조건을 설계할 수 있는 규칙을 제시했다.
또한 실험 결과를 실제 환자에게서 채취한 검체 120개에 적용한 결과, 약 20분 이내에 감염 여부를 판독했으며 정량 PCR(유전자 증폭 검사)과 유사한 수준의 정확도와 민감도를 보여, 기존 대비 신속하면서도 신뢰도 높은 진단이 가능함을 확인했다. 아울러 임상 적용 가능성도 입증했다.
이 기술은 특정 질병에 국한되지 않고 다양한 유전자 표적에 범용적으로 적용될 수 있다.
올리고의 설계를 조절하면 코로나19와 같은 감염병부터 각종 암 진단까지 다양한 분야에 적용할 수 있으며, 하나의 플랫폼으로 여러 질환을 진단할 수 있다.
또한 기존처럼 유전자마다 조건을 반복적으로 최적화할 필요가 없어 질환의 진단 설계를 단순화하고 개발 효율을 크게 높일 수 있다.
김민곤 교수는 “이번 연구는 특정 질환 하나를 위한 기술이 아니라, 다양한 유전자 표적에 맞춰 설계할 수 있는 진단 플랫폼의 가능성을 제시했다는 점에서 의미가 있다”며 “현재는 실제 감염병 환자 유래 샘플을 중심으로 성능을 검증했지만, 암·유전질환 등 다양한 분야로 확장 적용될 수 있을 것으로 기대한다”고 밝혔다.
GIST 화학과 김민곤 교수가 지도하고 박형빈 석박통합과정생이 제1저자로 참여한 이번 연구는 과학기술정보통신부·한국연구재단 글로벌연구네트워크사업 및 선도연구센터지원사업(IRC), 국가과학기술연구회(NST) 융합연구단 사업의 지원을 받았다.
연구 결과는 생화학 및 분자생물학 분야의 권위 있는 국제학술지《Nucleic Acids Research》에 2026년 3월 3일 온라인으로 게재됐다.
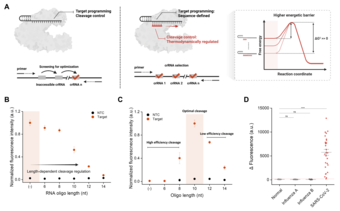
[그림] 유전자 가위(CRISPR) 기반 차세대 맞춤형 진단 플랫폼. 기존 유전자 가위 기술은 여러 조건을 바꿔서 맞추는 방식으로 진단을 만들어 시행착오가 많지만, 연구팀이 제시한 기술은 올리고를 통해 유전자 절단 속도를 조절해 더 쉽게 설계할 수 있다(A). 특히 올리고의 길이에 따라 유전자를 자르는 속도를 조절할 수 있고(B), 길이 조절을 통해 상황에 맞는 최적화된 진단이 가능하다(C). 연구팀은 실제 호흡기 바이러스 환자의 검체를 분석해 정확성을 입증했다(D).